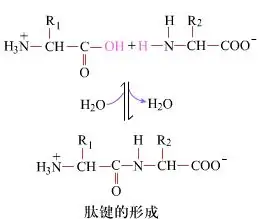
Na superficie, a formación de enlaces peptídicos, que producen dipéptidos, é un proceso químico sinxelo.Isto significa que os dous compoñentes de aminoácidos están unidos por un enlace peptídico, un enlace amida, mentres se deshidratan.
A formación de enlaces peptídicos é a activación dun aminoácido en condicións de reacción suaves.(A) fracción carboxilo, segundo aminoácido (B) O resto carboxilo activado nucleófilo forma entón o dipéptido (AB)."Se o compoñente carboxilo (A) non está protexido, a formación do enlace peptídico non se pode controlar".Os subprodutos como os péptidos lineais e cíclicos pódense mesturar cos compostos diana AB.Polo tanto, todos os grupos funcionais non implicados na formación de enlaces peptídicos deben estar protexidos de forma temporalmente reversible durante a síntese peptídica.
Así, a síntese peptídica - a formación de cada enlace peptídico - implica tres pasos de agregación.
O primeiro paso é preparar algúns aminoácidos que necesitan protección, e a estrutura zwitteriónica dos aminoácidos xa non existe.
O segundo paso é unha reacción en dúas etapas para formar enlaces peptídicos, na que primeiro se activa o grupo carboxilo do aminoácido N-protexido ao intermediario activo e despois fórmase o enlace peptídico.Esta reacción acoplada pode ocorrer como unha reacción dun paso ou como dúas reaccións secuenciais.
O terceiro paso é a eliminación selectiva ou eliminación completa da base protectora.Aínda que toda a eliminación só pode producirse despois de que todas as cadeas peptídicas foron ensambladas, tamén é necesaria a eliminación selectiva dos grupos protectores para continuar coa síntese peptídica.
Porque 10 aminoácidos (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec e Cys) conteñen grupos funcionais de cadea lateral, que requiren protección selectiva, facendo máis complicada a síntese de péptidos.Deben distinguirse as bases de protección temporal e semipermanente polos diferentes requisitos de selectividade.Os grupos de protección temporal utilízanse no seguinte paso para reflectir a protección temporal dos grupos funcionais de aminoácidos ou carboxilo.Os grupos protectores semipermanentes elimínanse sen interferir con enlaces peptídicos ou cadeas laterais de aminoácidos xa formados, ás veces durante a síntese.
"O ideal é que a activación do compoñente carboxilo e a posterior formación de enlaces peptídicos (reaccións de acoplamento) deberían ser rápidas, sen formación racémica nin de subprodutos, e deberían aplicarse reactivos molares para conseguir altos rendementos".Desafortunadamente, ningún dos métodos de acoplamento químico satisface estes requisitos, e poucos son axeitados para a síntese práctica.
Durante a síntese de péptidos, os grupos funcionais implicados en varias reaccións adoitan estar ligados ao centro manual, sendo a glicina a única excepción, e existe un risco potencial de rotación.
O paso final do ciclo de síntese do péptido é a eliminación de todos os grupos protectores.A eliminación selectiva de grupos protectores é importante para a extensión da cadea peptídica, ademais do requisito para a eliminación completa da protección na síntese de dipéptidos.As estratexias sintéticas deben ser coidadosamente planificadas.Dependendo da elección estratéxica, o N pode eliminar selectivamente os grupos protectores α-amino ou carboxilo.O termo "estratexia" refírese á secuencia de reaccións de condensación de aminoácidos individuais.En xeral, hai unha diferenza entre a síntese gradual e a condensación de fragmentos.A síntese de péptidos (tamén coñecida como "síntese convencional") ten lugar en solución.Na maioría dos casos, o alongamento gradual da cadea peptídica só se pode sintetizar usando a cadea peptídica para sintetizar fragmentos máis curtos.Para sintetizar péptidos máis longos, as moléculas diana deben segmentarse en fragmentos apropiados e determinar que poden minimizar o grao de diferenciación no extremo C terminal.Despois de que os fragmentos individuais sexan ensamblados gradualmente, o composto obxectivo unirase.A estratexia de síntese de péptidos inclúe a selección do fragmento protector mellor e máis apropiado, e a estratexia de síntese de péptidos inclúe a selección da combinación máis adecuada de bases protectoras e o mellor método de conxugación de fragmentos.
Hora de publicación: 19-Xul-2023